Enracinement des céréales : le minirhizotron pour étudier les racines in situ
Les plantes étant immobiles, l’adaptation de leur système racinaire est une stratégie capitale pour faire face aux variations temporelles et spatiales de la disponibilité de l’eau et des nutriments dans le sol.
Bien qu’elles soient des organes essentiels des plantes, les racines restent peu étudiées au champ car les méthodes d’échantillonnage racinaire de référence restent destructives. Parmi les méthodes non destructives, les minirhizotrons représentent l’option principale. Arvalis a évalué et développé des méthodes de phénotypage(1) racinaire au champ à l’aide de minirhizotrons en partenariat avec l’Inra d’Avignon et le Fonds de Soutien à l’Obtention Végétale.
Le système racinaire, acteur majeur d’une seconde « révolution verte »
L’introduction de variétés très efficientes en conditions de sols riches en nutriments, notamment à travers une résistance à la verse, a été la première de ces révolutions, opérée au milieu du XXe siècle. Cependant, l’essor de l’agriculture biologique et les incertitudes sur la durabilité des ressources minérales à la base des engrais conventionnels rendent à présent cruciale l’adaptation des futures variétés de céréales aux pratiques à faibles intrants. Les chercheurs australiens du CSIRO préconisent ainsi d’axer la sélection variétale sur les traits racinaires d’intérêt déjà identifiés ; ils soulignent la nécessité de développer des méthodes de phénotypage racinaire au champ.
La haute technologie au service de l’étude des racines
Le principe des minirhizotrons repose sur l’observation directe du système racinaire via un tube transparent inséré depuis la surface.
Les racines en contact avec les parois du tube sont alors observables, et il devient possible de quantifier leurs traits morphologiques. Les tubes sont isolés thermiquement dans leur partie émergée afin de réduire au mieux les effets de condensation. Les opérations nécessaires à la pose des minirhizotrons sont légères, mais les observations requièrent du matériel d’acquisition d’image adapté à un espace restreint.
« En donnant accès plus simplement à des caractères d’intérêt, les minirhizotrons ouvrent des pistes supplémentaires de sélection des variétés. »
Longtemps cantonnée à l’utilisation d’appareils photo combinés à des jeux de miroirs, la technologie d’acquisition d’images a peu à peu évolué, notamment avec l’emploi de caméras miniaturisées : les premiers véritables endoscopes racinaires. Ces dix dernières années, les progrès techniques ont permis d’augmenter la vitesse d’acquisition et ainsi que la résolution des images, en particulier grâce à l’émergence des systèmes de scanners rotatifs. Les capteurs CCD de ces scanners rotatifs sont capables de produire des images d’une résolution suffisante pour distinguer des détails jusqu’à 25 µm, soit moins que la moitié du diamètre d’un cheveu.
En pratique, les tubes transparents d’observations sont insérés dans le sol selon un angle de 30° à 45° par rapport à la verticale. Cette inclinaison réduit les biais de mesures obtenus avec des tubes parfaitement verticaux, les forages verticaux formant des « puits à racines » qui provoquent une croissance préférentielle. De plus, cet angle de pose permet d’échantillonner tout au long de la saison de culture les systèmes racinaires de plusieurs plantes à la fois, à travers les différentes profondeurs de sol traversées. Il est même possible de réaliser des suivis sur plusieurs années pour des problématiques spécifiques (agroforesterie ou écologie des prairies, par exemple).

Voir la plasticité racinaire
Les paramètres racinaires accessibles grâce aux minirhizotrons sont liés aux dimensions et aux positions des racines sur les images acquises.
Par exemple, la longueur cumulée des racines observées sur une image, rapportée à sa surface, donne une « densité de longueur racinaire », utilisée pour quantifier la colonisation du substrat par le système racinaire de la plante (figure 1).
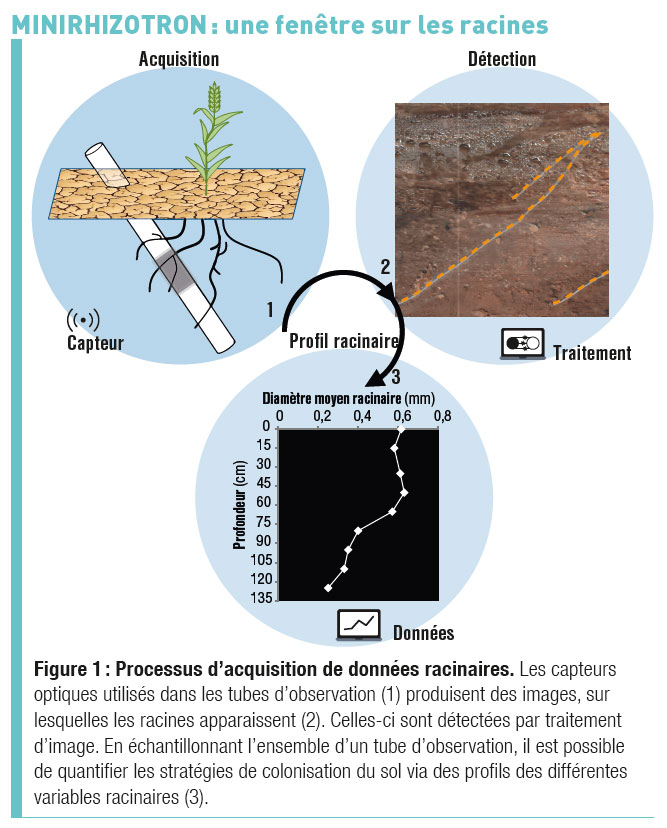
C’est ici que l’intérêt des minirhizotrons apparaît : puisque les densités de racines sont mesurées de façon répétée à différentes profondeurs en un même point, il est possible de quantifier l’allongement, la ramification et la mortalité des racines.
La plasticité du système racinaire face aux carences azotées peut notamment être étudiée, ainsi que les stratégies d’exploitation par les racines des réserves en eau du sol.
Comprendre les tolérances aux conditions limitantes
En effet, bien que la base génétique de la tolérance à la sécheresse du blé soit complexe et mal comprise, il a été démontré que les variétés récentes étaient mieux adaptées au déficit hydrique. L’architecture des racines est une piste potentielle d’amélioration de l’utilisation de l’eau par les cultures ; par exemple, des racines plus longues sont en mesure d’accéder à l’eau plus profondément dans le sol. De même, en cas de carence modérée en nutriments, le système racinaire des plantes tend à produire des racines plus fines et plus longues, maximisant le volume de sol exploré - notamment au-delà de 40 cm de profondeur chez une plante comme le blé. Ce type de réponse se manifeste par une augmentation du ratio « masse des parties racinaires sur masse des parties aériennes », et peut donc être estimé au champ avec des minirhizotrons puis quantifié plus précisément grâce à quelques mesures complémentaires. Ainsi, en instrumentant avec des minirhizotrons un essai agronomique appliquant des modalités d’apport d’azote différentes, il devient possible d’évaluer la réponse génétique à ce phénomène de développement préférentiel du système racinaire (figure 2).
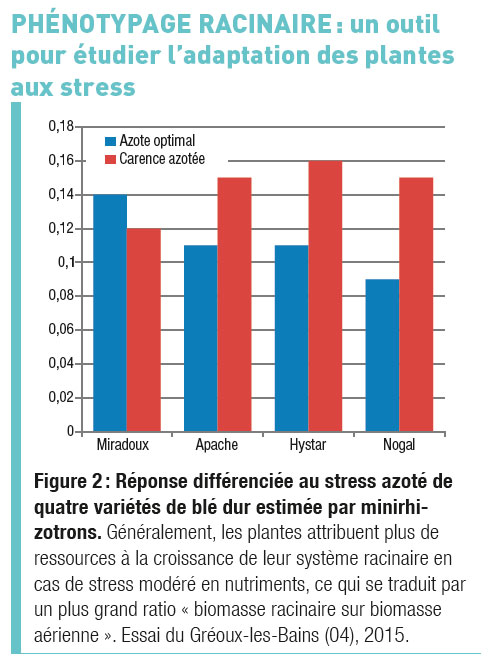
Les minirhizotrons introduisent des variables nouvelles, non accessibles par les anciens types d’échantillonnages destructifs. Ils donnent ainsi accès plus simplement à des caractères d’intérêt, et ouvrent des pistes de sélection supplémentaires pour répondre aux contraintes que l’agriculture du futur devra affronter. Parmi celles-ci, l’optimisation des diamètres racinaires : ceux-ci témoignent directement de l’efficacité de l’allocation des ressources de la plante, les diamètres les plus fins indiquant des racines plus longues pour autant de ressources mobilisées. Les diamètres racinaires interviennent aussi dans la colonisation des horizons de surface par les racines, généralement surabondantes (au-delà des densités requises pour extraire 100 % de l’eau disponible).
La technique doit néanmoins surmonter des freins techniques avant de pouvoir être exploitée à grande échelle, pour une activité expérimentale en réseau ou une distribution dans l’agrofourniture. Ainsi, les efforts d’Arvalis se concentrent sur l’automatisation du traitement des images acquises et son déploiement dans différentes architectures logicielles, afin de répondre aux besoins des nouvelles plateformes de recherches proposant un volet phénotypage racinaire à grande échelle - notamment celle de l’Inra de Dijon (Projet Carnot Plant2Pro 2018). Une fois levé un second verrou technologique (la mécanisation de l’installation des tubes d’observation couplés à des capteurs autonomes), la technique pourra s’inscrire dans le phénotypage dit « haut débit », liant agronomie et big data.
(1) Phénotyper les racines consiste à répertorier l’ensemble de leurs caractères apparents : longueur, section, nombre d’embranchements, position…




0 commentaire
Réagissez !
Merci de vous connecter pour commenter cet article.